骨髄異形成症候群
JALSG骨髄異形成症候群(MDS)の治療成績 (2012.8更新)
過去のMDSプロトコールの治療成績
JALSG MDS96 1)
【目的】
高リスクMDS(RAEB-t)およびMDS/AMLに対して、Ara-CとIDRを用いて寛解導入療法および寛解後療法を行い、本療法の有効性 および安全性を評価する。primary endpointは寛解率、secondary endpointは寛解期間、早期死亡率、再発率、生存期間、合併症の頻度、QOLとした。
【対象】
RAEB-tあるいはMDS/AML(MDSから移行のAML)と診断され、年齢が15歳以上70歳以下で、PSが0-2で、重要臓器に重篤な合併症を認めず、未治療の症例
【治療方法】
寛解導入療法として、AML95と同様、Ara-C+IDR療法(図1) を用いた。リスクファクターに基づいて投与量を
患者毎に調整する。リスクファクターとして、①年齢60歳以上、②骨髄低形成、③PSが2以上、を設定し、リスクファクターを有さない症例には標準投与量を用い、いずれか一つあれば標準量の80%投与量を用い、2つ以上あれば60%投与量に、それぞれ減量して 寛解導入を試みた。
地固め療法、維持/強化療法はJALSG AML95プロトコールに準じて、それぞれ3コース、6コースを施行するが、このときもリス クファクターによる減量計画に基づいて、患者毎に投与量を調整した。
【治療結果】
1996年6月から2000年11月まで、解析可能な登録症例は56例であった。年齢は17-68歳、男性36例、
女性20例であった。30 例に寛解が得られ、53.6%の寛解率であった。投与量別の症例数と寛解率および
寛解期間中央値は、それぞれ標準量投与群が30例で53.3%、259 日、80%投与量群が19例で47.4%、425日、そして60%投与量群が7例で71.4%、460日であった(表1)。症例数は少ないが、60%投与量群でも高い寛解率と長期の寛解期間が得られた。また、60%投与量群では、白血球最低値、白血球減少期間、血小板回復期間は標準量投与群と比べて有意差がなく、好中球の回復期間は短い傾向にあった(表2)。
高い寛解率と考え合わせると、リスクファクターによる減量を取り入れた治療計画は、
安全かつ有効に実施することができると考えられた。
高リスクMDS(RAEB-t)およびMDS/AMLに対して、Ara-CとIDRを用いて寛解導入療法および寛解後療法を行い、本療法の有効性 および安全性を評価する。primary endpointは寛解率、secondary endpointは寛解期間、早期死亡率、再発率、生存期間、合併症の頻度、QOLとした。
【対象】
RAEB-tあるいはMDS/AML(MDSから移行のAML)と診断され、年齢が15歳以上70歳以下で、PSが0-2で、重要臓器に重篤な合併症を認めず、未治療の症例
【治療方法】
寛解導入療法として、AML95と同様、Ara-C+IDR療法(図1) を用いた。リスクファクターに基づいて投与量を
患者毎に調整する。リスクファクターとして、①年齢60歳以上、②骨髄低形成、③PSが2以上、を設定し、リスクファクターを有さない症例には標準投与量を用い、いずれか一つあれば標準量の80%投与量を用い、2つ以上あれば60%投与量に、それぞれ減量して 寛解導入を試みた。
地固め療法、維持/強化療法はJALSG AML95プロトコールに準じて、それぞれ3コース、6コースを施行するが、このときもリス クファクターによる減量計画に基づいて、患者毎に投与量を調整した。
【治療結果】
1996年6月から2000年11月まで、解析可能な登録症例は56例であった。年齢は17-68歳、男性36例、
女性20例であった。30 例に寛解が得られ、53.6%の寛解率であった。投与量別の症例数と寛解率および
寛解期間中央値は、それぞれ標準量投与群が30例で53.3%、259 日、80%投与量群が19例で47.4%、425日、そして60%投与量群が7例で71.4%、460日であった(表1)。症例数は少ないが、60%投与量群でも高い寛解率と長期の寛解期間が得られた。また、60%投与量群では、白血球最低値、白血球減少期間、血小板回復期間は標準量投与群と比べて有意差がなく、好中球の回復期間は短い傾向にあった(表2)。
高い寛解率と考え合わせると、リスクファクターによる減量を取り入れた治療計画は、
安全かつ有効に実施することができると考えられた。
図1. JALSG MDS96 プロトコール
(寛解導入療法)
(寛解導入療法)
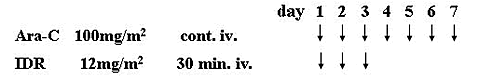
リスクファクターによる減量計画:
①年齢(60歳以上、 ②骨髄低形成、③PS(2以上)を設定し、リスクファクターのない症例には標準投与量を
用い、リスクファクターがいずれか一つあれば80%投与量を用い、2つ以上あれば60%投与量にそれぞれ減量する。
表1. 化学療法の投与量別寛解率と寛解期間
| 投与量 | 完全寛解患者数/ 治療を受けた患者数 (寛解率:%) |
寛解期間 (中央値:日) |
| 100% | 16/30(53.3%) | 259 |
80% |
9/19(47.4%) |
425 |
60% |
5/7(71.4%) |
460 |
30/56(53.6%) |
319 |
表2.寛解患者における血液毒性の投与量別比較
| 投与量 | 100% | 80% | 60% |
|---|---|---|---|
| 患者数 | 16 | 9 | 5 |
| 白血球最低値 (/μl) | 300 | 250 | 400 |
| 白血球1000 /μl以下の期間(日) | 17 | 18 | 15 |
| 好中球1000 /μlへの回復に要した日数(日) | 28 | 27 | 21 |
| 血小板10万 /μlへの回復に要した日数(日) | 30 | 27 | 30 |
| (中央値) |
JALSG MDS206 2)
【目的】
高リスクMDSおよびMDS/AMLの標準的治療法を確立し、Ara-C+IDR療法とAra-C+ACR併用(CA)療法
による寛解導入療法の 無作為割付による比較検討を行う。primary endpointは両群間の寛解率の比較、secondary endpointは寛解期間、早期死亡率、再発率、生存期間とした。
【対象】
IPSSでhighのMDSあるいはMDS/AML(MDSから移行のAML)と診断され、年齢が15歳以上で、PSが0-2で、重要臓器に重篤な合併症を認めず、未治療の症例
【治療方法】
寛解導入療法として、Ara-C+IDR療法とCA療法の割り付け(図2)を行った。MDS96同様、リスクファクター
に基づいて投与量を患者毎に調整する。地固め療法、維持/強化療法はJALSG AML95プロトコールに準じて、それぞれ3コース、6コースを施行する
【治療結果】
症例登録は2005年4月末で終了した。120例の登録があり、年齢中央値は、A療法群は63歳、B療法群で61歳であった。A療法群の寛解 率は、64.7%で、B療法群では43.9%であり、寛解期間は、320.6日と378.7日であった。
2年全生存率と無病生存率は、それぞれA療法群で28.1%と26.0%、B療法群では32.1%と24.8%であった(表3)。 いずれも統計学的に有意差を認めなかった。B療法群は、A療法群と比べて、寛解導入療法中の白血球減少期間は有意に短く、また感染合併も少なかったが、その他のGrade 3以上の有害事象に関しては、両療法群での有意差は認めなかった。今回の臨床試験から、強力化学療法により、寛解率が改善する傾向を認めたが、生存率の向 上にはつながらないことが示唆された。
高リスクMDSおよびMDS/AMLの標準的治療法を確立し、Ara-C+IDR療法とAra-C+ACR併用(CA)療法
による寛解導入療法の 無作為割付による比較検討を行う。primary endpointは両群間の寛解率の比較、secondary endpointは寛解期間、早期死亡率、再発率、生存期間とした。
【対象】
IPSSでhighのMDSあるいはMDS/AML(MDSから移行のAML)と診断され、年齢が15歳以上で、PSが0-2で、重要臓器に重篤な合併症を認めず、未治療の症例
【治療方法】
寛解導入療法として、Ara-C+IDR療法とCA療法の割り付け(図2)を行った。MDS96同様、リスクファクター
に基づいて投与量を患者毎に調整する。地固め療法、維持/強化療法はJALSG AML95プロトコールに準じて、それぞれ3コース、6コースを施行する
【治療結果】
症例登録は2005年4月末で終了した。120例の登録があり、年齢中央値は、A療法群は63歳、B療法群で61歳であった。A療法群の寛解 率は、64.7%で、B療法群では43.9%であり、寛解期間は、320.6日と378.7日であった。
2年全生存率と無病生存率は、それぞれA療法群で28.1%と26.0%、B療法群では32.1%と24.8%であった(表3)。 いずれも統計学的に有意差を認めなかった。B療法群は、A療法群と比べて、寛解導入療法中の白血球減少期間は有意に短く、また感染合併も少なかったが、その他のGrade 3以上の有害事象に関しては、両療法群での有意差は認めなかった。今回の臨床試験から、強力化学療法により、寛解率が改善する傾向を認めたが、生存率の向 上にはつながらないことが示唆された。
図2. JALSG MDS200 プロトコール
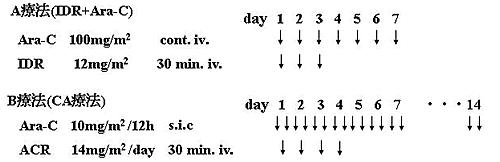
●無作為にA群またはB群に割り付けを行う
●A療法はリスクファクターによる減量計画に従って投与量を調節する。
●B療法はG-CSFを併用するCAG療法を行ってもよい。
地固め療法および維持・強化療法
A群およびB群ともにJALSG-AML95のプロトコールに準じて行う。
表3.A療法(Ara-C +IDR)群とB療法(Ara-C+ACR)群との治療成績比較
| A療法群(53例) | B療法群(67例) | |
|---|---|---|
| 寛解率(60%) | 64.7 | 43.9 |
| 寛解期間平均値(日) | 320.6 | 378.7 |
| 2年全生存率(%) | 28.1 | 32.1 |
| 2年無病生存率(%) | 26.0 | 24.8 |
表4.寛解導入療法での有害事象の比較
*有意差あり
| A療法群(53例) | B療法群(67例) | |
|---|---|---|
| 白血球減少(1000未満)期間*(日) | 19(0~44) | 4(0~50) |
| 有害事象(Grade 3/4) あり 出血 感染* |
19 2 17 |
13 1 11 |
| 早期死亡(30日以内) | 1 | 3 |
文献
1) Okamoto T, et al.: Combination chemotherapy with risk
factor-adjusted dose attenuation for high-risk myelodysplastic syndrome
and resulting leukemia in the multicenter study of the Japan Adult
Leukemia Study Group (JALSG): results of an interim analysis. Int J
Hematol 2000;72: 200-205.
2) Morita Y, et al.: Comparative analysis of remission induction therapy for high-risk MDS and AML progressed from MDS in the MDS200 study of Japan Adult Leukemia Study Group. Int J Hematol 2010;91:97-103.
2) Morita Y, et al.: Comparative analysis of remission induction therapy for high-risk MDS and AML progressed from MDS in the MDS200 study of Japan Adult Leukemia Study Group. Int J Hematol 2010;91:97-103.
